撰文:核子醫學科 黃玉儀主任
Prostate-specific membrane antigen (PSMA)因對攝護腺癌細胞的高度特異性及結合力,是目前公認偵測攝護腺癌淋巴結以及遠端轉移的最佳工具。
Ga-68-PSMA-11 PET使用經驗最多,研究成果最完整
作為初診斷分期,Ga-68-PSMA-11 PET 的敏感性及特異性分別為74%及96%,當PSA >2 ng/mL時,偵測率高達94%,而在PSA <2 ng/mL的狀況下,仍有67%的病人能藉由Ga-68-PSMA-11 PET 檢查偵測到復發或轉移病灶。高風險攝護腺癌病人在手術前進行Ga-68-PSMA-11 PET 檢查,也被發現較傳統的影像學檢查(如CT, MRI,或骨骼掃描)有更高的正確度。2022年一篇針對2005位經初步治癒性治療後PSA上升的病人進行的大型研究再次確認,PSA >2 ng/mL時,Ga-68-PSMA-11 PET 偵測率即可超越90%,在0.5~2 ng/mL的情況下,可有超過70%的偵測率。現行Lu-177-PSMA治療前的診斷評估,也都是以Ga-68-PSMA-11 PET作為標準研究工具。目前Ga-68-PSMA-11 PET 是使用經驗最多,研究成果最完整的攝護腺癌診療用正子掃描。
除了以放射性正子同位素Ga-68標記的PSMA-11外,陸續開始有了以正子同位素F-18標記的PSMA製劑。F-18同位素的優點是半衰期較長,藥物效力可維持較久,適合異地製作運輸,可使用較足量的藥劑,造影品質更佳,但是藥物分布特性與Ga-68標記的PSMA-11可能會稍有不同。研究資料較多的有三種藥物,F-18-DCFPyL(商品名Pylarify)、F-18-PSMA-1007,以及2023年後問世的F-18-flotufolastat(保攝樂,Posluma)。其中F-18-DCFPyL的藥物分布特性與Ga-68-PSMA-11較為接近,然而目前台灣尚無法取得。
F-18-PSMA-1007 PET 具優異的影像品質以及偵測率,但假陽性率偏高
F-18-PSMA-1007是在歐洲藥典正式收錄的F-18標記的PSMA製劑,台灣已有幾家正子中心具備製藥能力,也是台灣攝護腺癌病人的檢查選項之一。由於在尿液中的代謝量極低,因此F-18-PSMA-1007 PET 有相當優異的影像品質以及偵測率, PSA >1 ng/mL時,即可有超過90%的機會發現復發病灶,在0.5~1 ng/mL的情況下,可有超過70%的偵測率,是攝護腺癌病人懷疑復發時非常好的檢查選項,但是必須要注意F-18-PSMA-1007 PET偏高的假陽性率,主要發生於骨骼以及神經節的部位。F-18-PSMA-1007 PET另一個限制肝臟的代謝量高,因此可能更不容易偵測到肝臟的轉移病灶。一項比較性研究發現,102位懷疑攝護腺癌復發的病人同時接受F-18-PSMA-1007 及Ga-68-PSMA-11兩種PET檢查,F-18-PSMA-1007 PET發現的369個病灶中僅有124處確實是攝護腺癌的轉移病灶,假陽性的病灶數量幾乎是真實病灶數量的兩倍,而同樣這些病人進行Ga-68-PSMA-11檢查,則是發現178個病灶,其中126處確實是攝護腺癌的轉移病灶。(圖一)
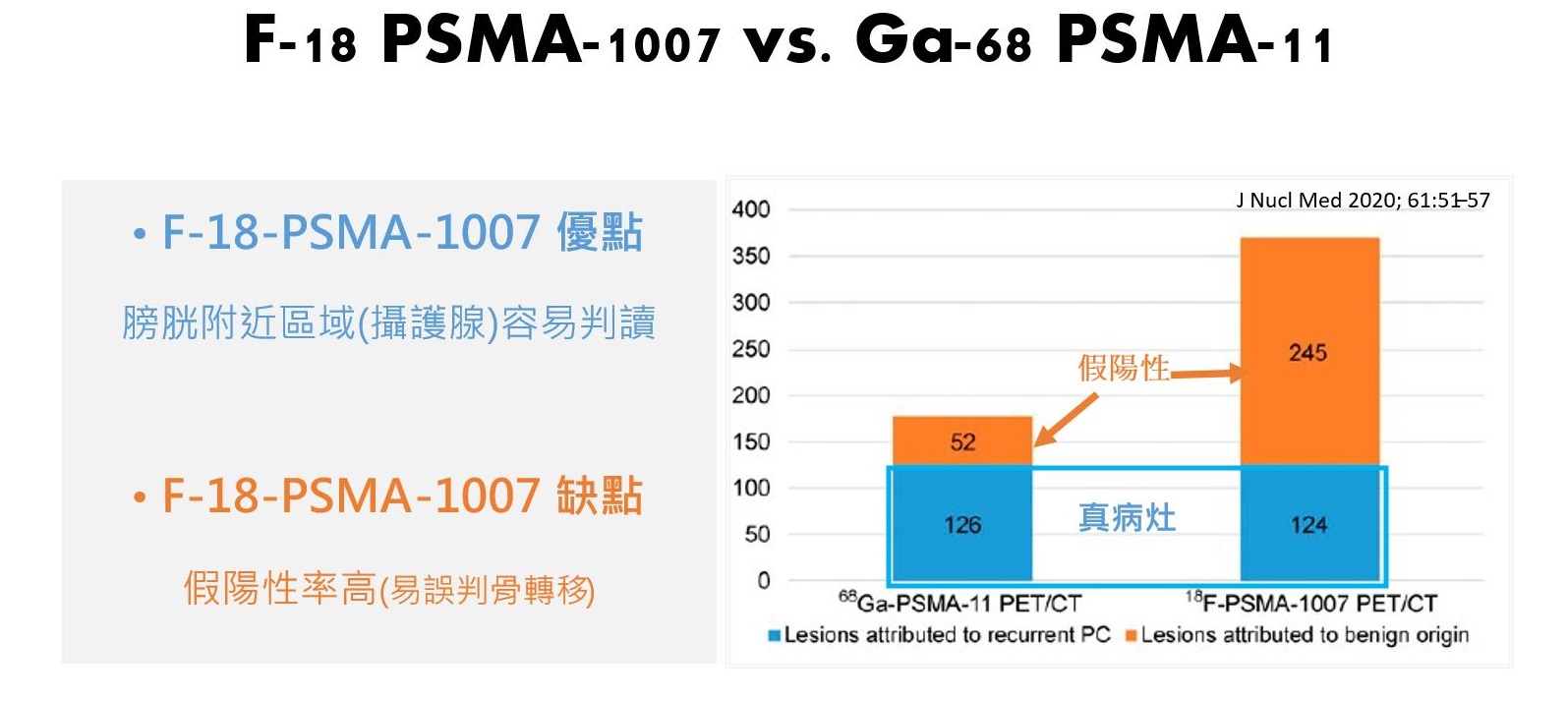
圖一、F-18-PSMA-1007 及Ga-68-PSMA-11兩種PET檢查,F-18-PSMA-1007 PET發現的369個病灶中僅有124處確實是攝護腺癌的轉移病灶。
另一篇研究則發現,F-18-PSMA-1007 PET懷疑的11處骨轉移,經切片確認後,僅1處證實真的是攝護腺癌的轉移,其餘10處皆為假陽性。(圖二)
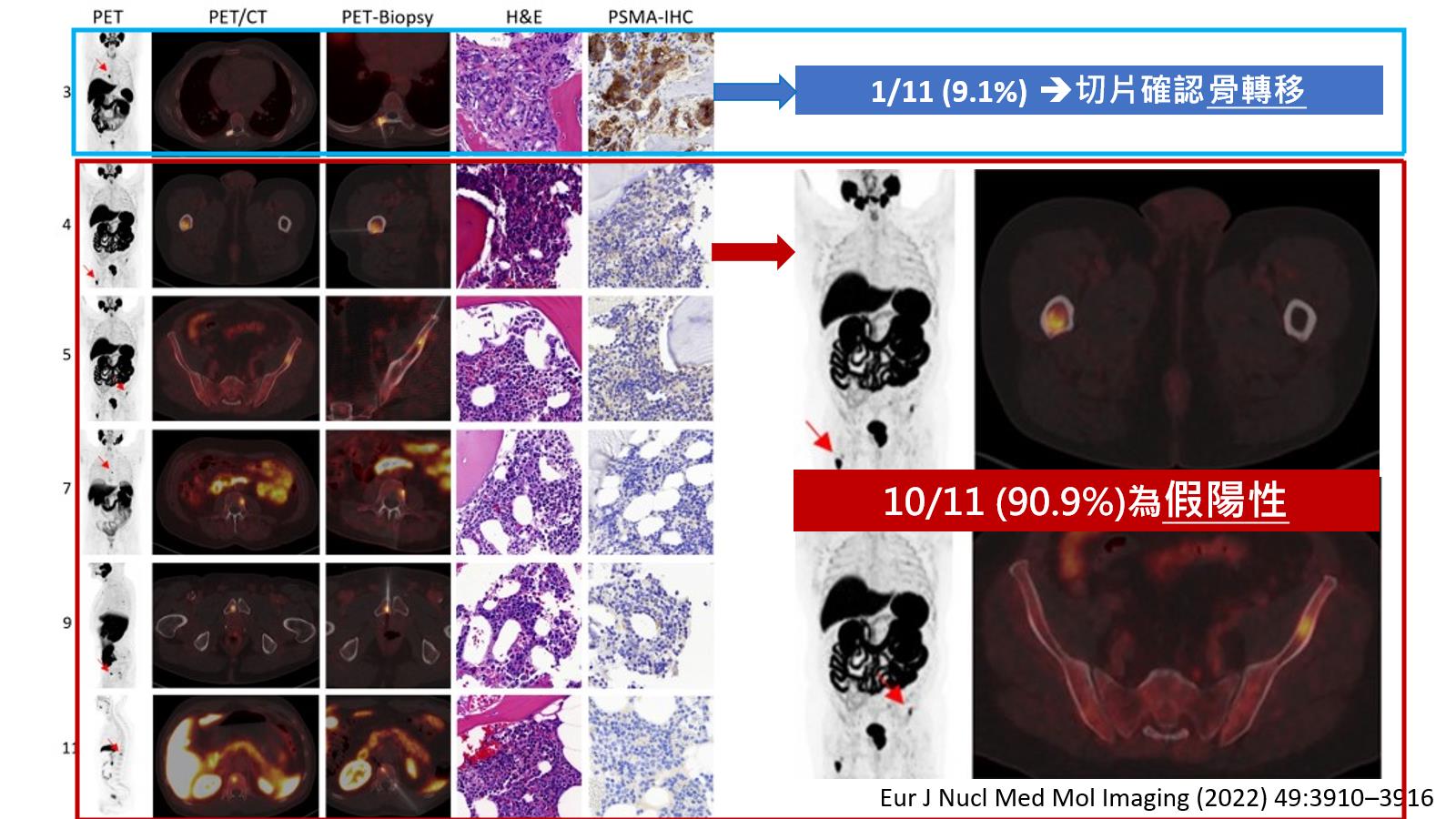
圖二、F-18-PSMA-1007 PET懷疑的11處骨轉移,經切片確認後,僅1處證實真的是攝護腺癌的轉移,其餘10處皆為假陽性。
由於前述的這兩項限制,我個人認為F-18-PSMA-1007 PET可用於懷疑復發的偵測,但較不建議使用在攝護腺癌初診斷高風險分期時使用,因為過於常見的骨骼假陽性病灶可能會剝奪了病人接受積極治癒性治療的機會。
2025年12月更新:F-18-flotufolastat(保攝樂,Posluma) - 取得食藥署核發藥品許可證之F-18 PSMA靶向PET製劑
F-18-flotufolastat近年發展的新型 F-18 標記 PSMA PET 造影劑,商品名為Posluma,台灣中文名為「保攝樂」,由Blue Earth Diagnostics(Bracco旗下公司)開發,研發代號原稱18F-rhPSMA-7.3。此藥於2023年5月獲美國FDA核准,由臺灣新吉美碩股份有限公司(GMS Taiwan)負責台灣地區之製造與供應,並於2025年12月取得台灣衛生福利部食品藥物管理署核發的藥品許可證,代表此藥品已完成在台灣上市使用的核准程序。這與部分醫療機構依規定通過院內正子藥品調製查核不同;前者是藥品本身的上市許可,後者是特定醫療機構調製作業的核准。保攝樂因F-18半衰期較長的優勢,利於藥物長程配送,可使更多醫療院所有機會提供此項檢查,有助於提升台灣攝護腺癌病人接受 PSMA PET 檢查的可近性。Posluma採用獨特的「放射混合(Radiohybrid, rh)技術」,最大特點是尿液排泄量極低,注射後2小時內約僅7%由尿液排出,使膀胱及泌尿道的放射性干擾大幅降低。這一特性在攝護腺切除術後的骨盆腔復發偵測上尤具優勢,有機會更清晰顯示攝護腺窩附近的細微病灶。臨床數據方面,核准依據為兩項第三期試驗SPOTLIGHT(生化復發)與LIGHTHOUSE(初診斷分期)。SPOTLIGHT試驗中之整體偵測率達83%(389 位可評估病人),而根據Rauscher 等人的回顧性研究報告 PSA <1 ng/mL 的 18F-rhPSMA-7.3 偵測率約 62–68%,0.5–<1 ng/mL = 67.9%,PSA 0.2–<0.5 ng/mL = 61.8%。LIGHTHOUSE試驗中高風險病人術前骨盆腔淋巴結偵測特異性達93-97%。
各種PSMA靶向PET製劑的比較
以上提到的幾種PSMA靶向PET製劑各有優缺點,大家可以參考:
- 影像比較(圖三)
- 核准狀態及適應症等比較說明(表一) (註:在台灣,PSMA PET 製劑的法規狀態可分為兩種情況。第一種是藥品本身取得食藥署核發的藥品許可證,代表該藥品已完成上市使用的核准程序;第二種是醫療機構依《正子藥品優良調劑作業準則》通過特定品項的院內調製查核,代表該醫療機構可在符合規範的條件下調製該正子藥品。兩者都屬於食藥署管理,但意義不同,前者是「藥品上市許可」,後者是「特定機構的調製作業核准」。)
- 建議使用時機(圖四)。
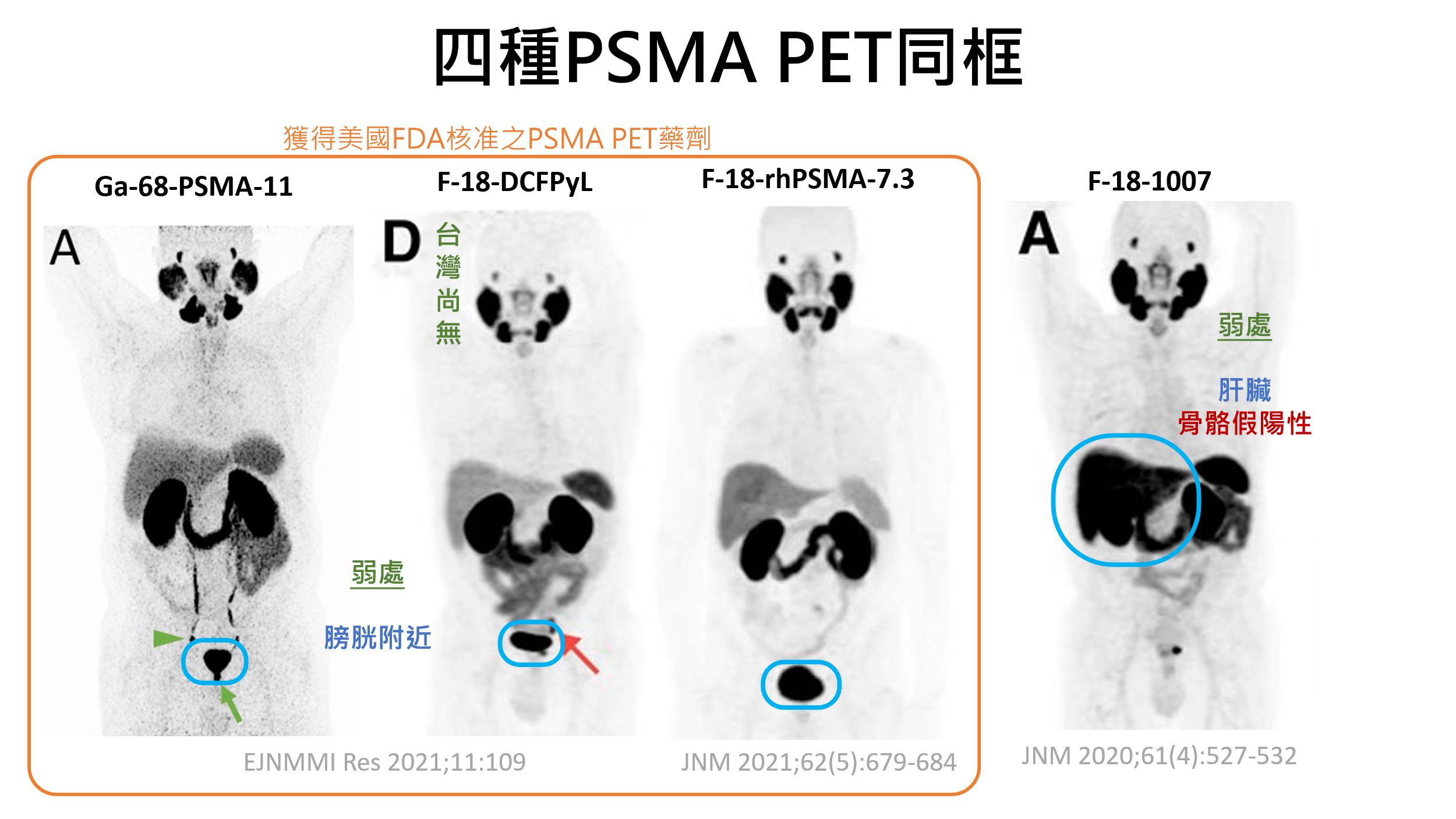
圖三、臨床可用的四種PSMA PET
表一、各種PSMA PET製劑比較
| PSMA PET 製劑 | 標記同位素 | 美國 FDA 狀態 | 台灣狀態 | 常見使用情境 | 主要優點 | 注意事項 |
|---|---|---|---|---|---|---|
| Ga-68-PSMA-11 | Ga-68 | 美國已有 Ga-68 gozetotide 相關核准產品;Locametz 核准用途包括初診斷分期、生化復發,以及 Lu-177 vipivotide tetraxetan 治療前選病人。(FDA Access Data) | 多由醫療機構自行合成/調製,需依規定通過正子藥品調製查核(不同於一般藥品許可證)。 | 初診斷高風險分期、生化復發、Lu-177-PSMA 治療前評估 | 臨床經驗最久、文獻最完整,許多 Lu-177-PSMA 臨床試驗以此作為選病人工具 | 半衰期較短,通常需院內或鄰近地點可製備 |
| F-18-DCFPyL (Pylarify) | F-18 | FDA 核准用於疑似轉移且適合初次決定性治療者,以及 PSA 上升懷疑復發者。(FDA Access Data) | 目前台灣臨床上尚非可取得選項 | 初診斷分期、生化復發 | 分布特性與 Ga-68-PSMA-11 較接近;F-18 半衰期較長,利於配送 | 台灣無法取得 |
| F-18-flotufolastat (Posluma/保攝樂) | F-18(radiohybrid)技術 | FDA 核准用於疑似轉移且適合初次決定性治療者,以及 PSA 上升懷疑復發者。(FDA Access Data) | 已取得台灣藥品許可證,衛部藥製字第 R00049 號。 | 初診斷分期、生化復發;是否作為治療前評估需依治療藥品仿單、臨床指引與醫師判斷 | 尿液排泄比例低,注射後前 2 小時約 7% 經尿液排出,有助於降低膀胱與泌尿道背景干擾。(FDA Access Data) | 台灣臨床經驗仍在累積 |
| F-18-PSMA-1007 | F-18 | 未獲 FDA 核准 | 台灣部分正子中心可依醫療機構調製查核方式提供(不同於一般藥品許可證)。 | 生化復發偵測,尤其骨盆腔局部復發評估 | 尿液排泄少,骨盆腔影像背景較乾淨 | 骨骼與神經節假陽性較需小心;肝臟背景較高,肝轉移偵測可能受影響 |

圖四、各種PSMA PET的建議使用時機。








