從臨床故事走進李-佛美尼症候群 (Li-Fraumeni) 症候群的分子世界
她第一次罹癌時,才二十七歲。那一年,她被診斷為左側乳癌。隔年,右側乳癌接踵而至。醫療團隊依循當時最標準的治療路徑:手術、化學治療、放射線治療、內分泌治療。她活了下來,努力回到生活的軌道。沒有人在那個時候,將「遺傳性癌症症候群」放在鑑別診斷的前列。
直到時間開始以不尋常的方式加速。四十五歲,左側乳房再次出現新的原發癌。四十七歲,她同時被診斷為食道腺癌與早期膽囊癌;四十八歲,子宮內膜混合型癌症確診。她的婦科醫師王宗德醫師,看了她有過這樣多重原發癌、年輕發病、橫跨不同器官系統——這些線索逐漸拼湊出一個熟悉卻罕見的臨床輪廓,懷疑很可能有遺傳性的基因變異。他花時間說服病人進行遺傳性基因檢測,如果能找到基因的變異,可對將來的癌症進行預防,避免發現時已轉移或無法治療。如果確定是遺傳,也可以對父母、兄弟姊妹、兒女進行篩檢,避免將來家族罹癌的悲劇。跟病人解釋遺傳性基因的檢測需要耐心說明與真心願意照顧病人的醫師。
然而這不是偶然。
TP53 變異的灰色地帶
2025 年 11 月,她接受了 Invitae公司遺傳性多癌症 「次世代基因定序 (NGS) 廣泛型檢測。她的報告:未檢出明確致病突變。但在細節中,藏著關鍵訊息。 她攜帶一個 TP53 雜合性變異:c
同時,她的子宮內膜癌腫瘤組織呈現 p53 基因變異免疫染色型態,它暗示這是 TP53 功能喪失在腫瘤生成中的真實角色。這正是李-佛美尼症候群(Li-Fraumeni, LFS)在現代醫學中最具挑戰性的面貌之一:基因報告尚未給出「確診」,但臨床證據已經指向答案。
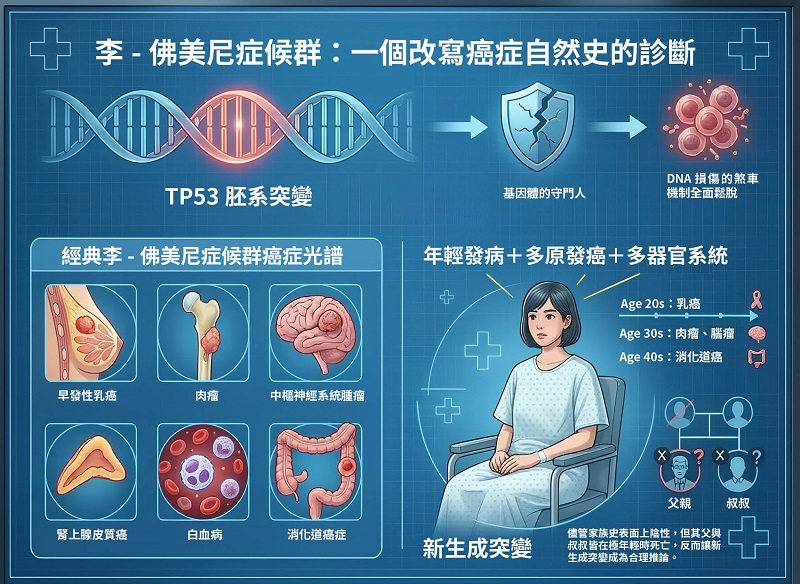
李-佛美尼症候群:一個改寫癌症自然史的診斷
李-佛美尼症候群(LFS)是一種由 TP53 胚系突變所造成的高度致癌體質。TP53 被稱為「基因體的守門人」,一旦失能,細胞會對 DNA 損傷的煞車機制便全面鬆脫。經典李-佛美尼症候群 的癌症光譜包括:早發性乳癌、肉瘤、中樞神經系統腫瘤、腎上腺皮質癌、白血病、消化道癌症。
在這位女性身上,幾乎完整呈現了 「年輕發病+多原發癌+多器官系統」 的典型臨床表型。儘管家族史表面上陰性,但其父親與叔叔皆在極年輕時死亡,反而讓新生成突變成為合理推論。
「尚未確診」不代表「可以等待」
- 精準醫學不是只看基因結果,而是將基因、腫瘤表現與臨床歷程整合判讀。
在這個案例中:
- 多個腫瘤呈現 p53 變異表現型
- 發病年齡顯著早於一般族群
- 癌症型態高度符合 LFS 光譜
- TP53 變異具高度功能破壞預測
因此,即使 TP53 仍被標示為尚未確定為明確致病突變,臨床上已足以「以李-佛美尼症候群的標準進行管理」。這不是過度治療,而是風險治理。
管理的核心,不是治療,而是「避免傷害」
對 LFS 病人而言,醫療策略的第一原則不是「積極治療」,而是避免任何可能加速第二原發癌的醫療傷害。依據美國國家綜合癌症網絡《遺傳/家族高風險評估》最新版建議,重點包括:
一、避免輻射
- 盡量避免放射線治療
- 最小化診斷性輻射暴露
二、主動監測,而非被動等待
- 每年全身 MRI
- 每年腦部 MRI
- 每 3–4 個月 CBC(白血病監測)
- 每 2–5 年大腸鏡與上消化道內視鏡
- 乳房:每年 MRI ± 乳房攝影,並討論預防性切除
- 每 6–12 個月完整理學檢查
- 每年皮膚檢查
這些檢查的目的,不是增加焦慮,而是將癌症從「突襲」轉為「早期可控事件」。
一個仍在進行中的故事
這位女性的故事尚未結束。她的 TP53 變異仍在等待科學給出最終答案。這正是李-佛美尼症候群Li-Fraumeni 症候群在 21 世紀的真正意義。不是一個診斷名稱,而是一場結合臨床直覺、分子證據與長期醫療觀察的醫學實踐。(Patient : 03590312 )








